上海交大代彬团队在石墨烯量子点调控蛋白异常相分离研究中取得重要突破
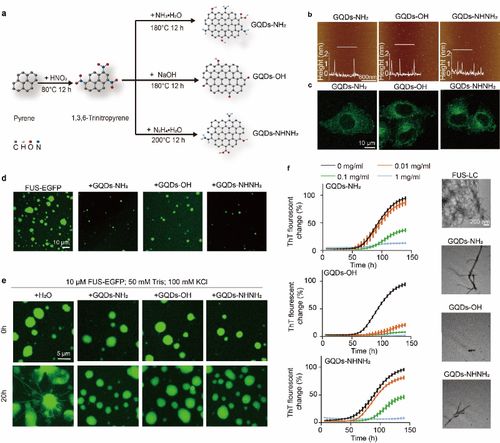
上海交通大学生物医学工程学院及材料科学与工程学院代彬教授团队在《自然·通讯》(Nature Communications)期刊上发表了一项前沿研究成果。该研究深入探讨了石墨烯量子点(GQDs)对蛋白质异常相分离(aberrant phase separation)的调控作用及其分子机制,为神经退行性疾病如阿尔茨海默病、帕金森病等的病理研究与潜在干预策略开辟了全新视角。
蛋白质相分离是细胞功能调控的基本物理化学过程。在特定病理条件下,某些蛋白质(如FUS、TDP-43等)会发生异常相分离,形成具有细胞毒性的凝胶或固体聚集体,进而导致神经元功能障碍甚至死亡,这是多种神经退行性疾病的共同病理特征之一。因此,寻找能够精准调控这一过程的分子工具,具有重要的科学意义与临床价值。
代彬团队创新性地将目光投向了纳米材料领域。石墨烯量子点是一种尺寸在10纳米以下、具有优异光学特性、良好生物相容性和可功能化表面的碳基纳米材料。研究人员通过精确调控GQDs的表面化学性质(如官能团、电荷分布),系统研究了不同GQDs与易发生异常相分离的病理蛋白模型(如FUS蛋白的低复杂度结构域)的相互作用。
研究结果表明,特定表面修饰的GQDs能够有效抑制病理蛋白的异常相分离过程。其作用机制主要包括:
- 动态干扰:GQDs通过π-π堆积、静电相互作用或氢键等方式,与蛋白质中驱动相分离的关键结构域结合,干扰其多价相互作用网络,从而抑制异常凝聚体的形成。
- 溶解已形成的聚集体:对于已经形成的蛋白质凝胶或固态聚集体,某些类型的GQDs能够渗入其中,破坏其内部相互作用,促使其解聚或转化为流动性更强的液态微滴。
- 调节相行为:GQDs能够改变蛋白质相分离的“相图”,提高其发生异常相分离的能量壁垒,从热力学上稳定蛋白质的溶解态。
该研究的亮点在于,团队不仅揭示了GQDs的调控能力,更通过多尺度模拟(分子动力学模拟等)与高分辨显微成像技术(如荧光共聚焦显微镜、原子力显微镜)相结合,在分子和纳米尺度上阐明了相互作用的动态细节,为“材料-生物界面”的精准设计提供了理论依据。
此项研究属于“自然科学研究和试验发展”的重要范畴,它成功跨越了材料科学、生物物理与神经生物学等多个学科边界,展示了一种利用功能性纳米材料干预基础生命过程的创新范式。基于石墨烯量子点的可调控性,研究人员有望开发出针对特定病理蛋白的“纳米调控剂”,为神经退行性疾病的诊断与治疗提供全新的工具和思路。代彬团队的工作,标志着我国在生物材料与疾病交叉研究领域取得了又一项具有国际影响力的进展。
如若转载,请注明出处:http://www.zxxjsks.com/product/50.html
更新时间:2026-04-14 07:15:14